Introduzione
Le infezioni cutanee rappresentano una seria minaccia per la salute animale, diffusa a livello globale. Più in particolare, gli animali da allevamento di grande taglia, quali i bovini, possono periodicamente soffrire di patologie di varia natura di tipo infettivo a livello cutaneo o dello zoccolo, con decorsi lenti e di difficile soluzione, e che, nelle situazioni peggiori, possono condurre a conseguenze gravi e all’eliminazione dell’animale. Tali patologie rappresentano quindi un rischio per il benessere e la salute degli animali, oltre a dare luogo ad evidenti svantaggi economici. Non sorprende, perciò, che sul mercato esistano numerose preparazioni per la cura della cute e dello zoccolo degli animali da reddito. Vi è tuttavia una crescente preoccupazione in merito ad alcune di queste preparazioni in quanto loro componenti, o eventuali loro metaboliti, possono risultare variamente tossici per l’animale trattato e comportare problemi per il loro smaltimento nell’ambiente.
Per la cura delle infezioni dello zoccolo bovino sono stati storicamente usati i bagni podalici con formalina o con solfato di rame, oppure, sia nel caso dello zoccolo che della cute, composti a base di tetracicline, oltre a pomate contenenti, ad esempio, zinco, rame o zolfo. Nell’Unione europea, nonostante la formalina sia attualmente approvata come principio attivo nella categoria biocidi, il suo utilizzo è motivo di preoccupazione e oggetto di dibattito, essendo classificata tra gli agenti cancerogeni (regolamento di esecuzione UE n. 2020/1763 del 25 novembre 2020). Inoltre, alcuni paesi importatori di formaggio, come ad esempio USA, Giappone e Russia, disincentivano o vietano latticini derivanti da latte ottenuto da animali sottoposti a trattamenti con antibiotici, quali le tetracicline.
Un problema ancora più preoccupante è rappresentato dalla resistenza sviluppata da molti microrganismi ai comuni disinfettanti. Ad esempio, infezioni da Staphylococcus aureus non vengono risolte dall’applicazione dei più diffusi antisettici, quali la clorexidina. Di conseguenza, è fortemente percepita l’esigenza da parte degli stakeholders, quali gli operatori del settore e le aziende, di nuove proposte nel campo della disinfezione degli animali, che si riflette nell’urgente richiesta di alternative competitive alle sostanze attualmente utilizzate per la cura della cute degli animali da reddito [Hajipour et al., 2012]. In questo contesto, l’uso di materiali colloidali rappresenta una delle idee scientifiche più rivoluzionarie [Pelgrift et al., 2013]. Nello specifico, gli ossidi di ferro colloidali forniscono un’ampia gamma di vantaggi, tra i quali l’elevata biocompatibilità e le elevate proprietà ossido-riduttive [Magro et al., 2016] che permettono a questi materiali di produrre localmente specie reattive dell’ossigeno (ROS). Tali caratteristiche fanno intravedere un loro potenziale impiego nel campo delle terapie topiche [Mai et al., 2017].
Il team di ricerca di AINT s.r.l. (Advanced Iron NanoTechnologies, spin off dell’Università di Padova), presso i laboratori del Dipartimento di Biomedicina Comparata e Alimentazione dell’Università degli Studi di Padova, ha maturato una notevole esperienza nel campo della sintesi e della caratterizzazione di ossidi metallici, con applicazioni in ambito biotecnologico e biomedicale che sono state pubblicate in riviste internazionali ad elevato impatto [Basso et al., 2019; Magro et al., 2017; Magro et al., 2019]. Recentemente, nel corso dell’attività di ricerca è stata sviluppata una sospensione colloidale di ossidi di ferro, contenente acidi organici e detergenti, in grado di catalizzare efficacemente l’eliminazione dei microrganismi dalla superficie cutanea degli animali. La suddetta formulazione è stata studiata per sviluppare un’azione battericida molto localizzata, e può quindi essere vantaggiosamente utilizzata per applicazioni di tipo topico. Tale formulazione è in grado di ripulire rapidamente gli zoccoli ed eliminare le impurità superficiali della pelle, le cellule morte e desquamate, assicurando un’azione preventiva per la ricomparsa di carie agli zoccoli e di micosi cutanee. Il prodotto, inoltre, presenta l’ulteriore vantaggio di non venire assorbito, di essere inodore e di non macchiare.
L’innovatività dell’invenzione di AINT s.r.l. è stata recentemente confermata dall’ufficio brevetti europeo (European Patent Office, EPO), che ne ha concesso il brevetto (n. EP3328366 del 2020). Nello specifico, l’EPO ha riconosciuto come innovativa l’azione sinergica dell’effetto combinato dei componenti della formulazione che sono in grado di “catalizzare” efficacemente ed in modo aspecifico l’eliminazione dei microrganismi. Il preparato, che attualmente è proposto in commercio da AINT con la denominazione IRON ANIMALS, rappresenta un’alternativa davvero competitiva rispetto alle sostanze attualmente utilizzate per la cura della cute animale.
L’efficacia di IRON ANIMALS è stata dimostrata da un team di ricerca interdisciplinare guidato dal Prof. Maurizio Isola del Dipartimento di Medicina, Produzione e Salute Animale dell’Università di Padova, che ha visto il coinvolgimento di veterinari, microbiologi e biochimici. Lo studio è stato oggetto di una pubblicazione scientifica intitolata “Colloidal iron oxide formulation for equine hoof disinfection” su “Animals” (ISSN 2076-2615) [Isola et al., 2021]. Lo studio di Isola ha dimostrato la capacità di IRON ANIMALS di superare i limiti dei comuni disinfettanti e, in particolare, di eliminare completamente microrganismi dannosi ed estremamente resistenti, come lo Staphylococcus aureus dallo zoccolo equino.
In ambito bovino, IRON ANIMALS è stato utilizzato sul campo con successo risolvendo annose condizioni patologiche, quali la dermatite digitale ed interdigitale, le dermato-tricosi del mantello (tricofizie) e le piaghe mammarie posizionate lungo il legamento e/o nella zona di contatto con la coscia.
Risultati
Azione battericida in vitro
L’effetto battericida dell’ossido di ferro colloidale è stato testato su batteri sia Gram-positivi (due ceppi di Staphylococcus aureus) che Gram-negativi (due ceppi di Pseudomonas aeruginosa).
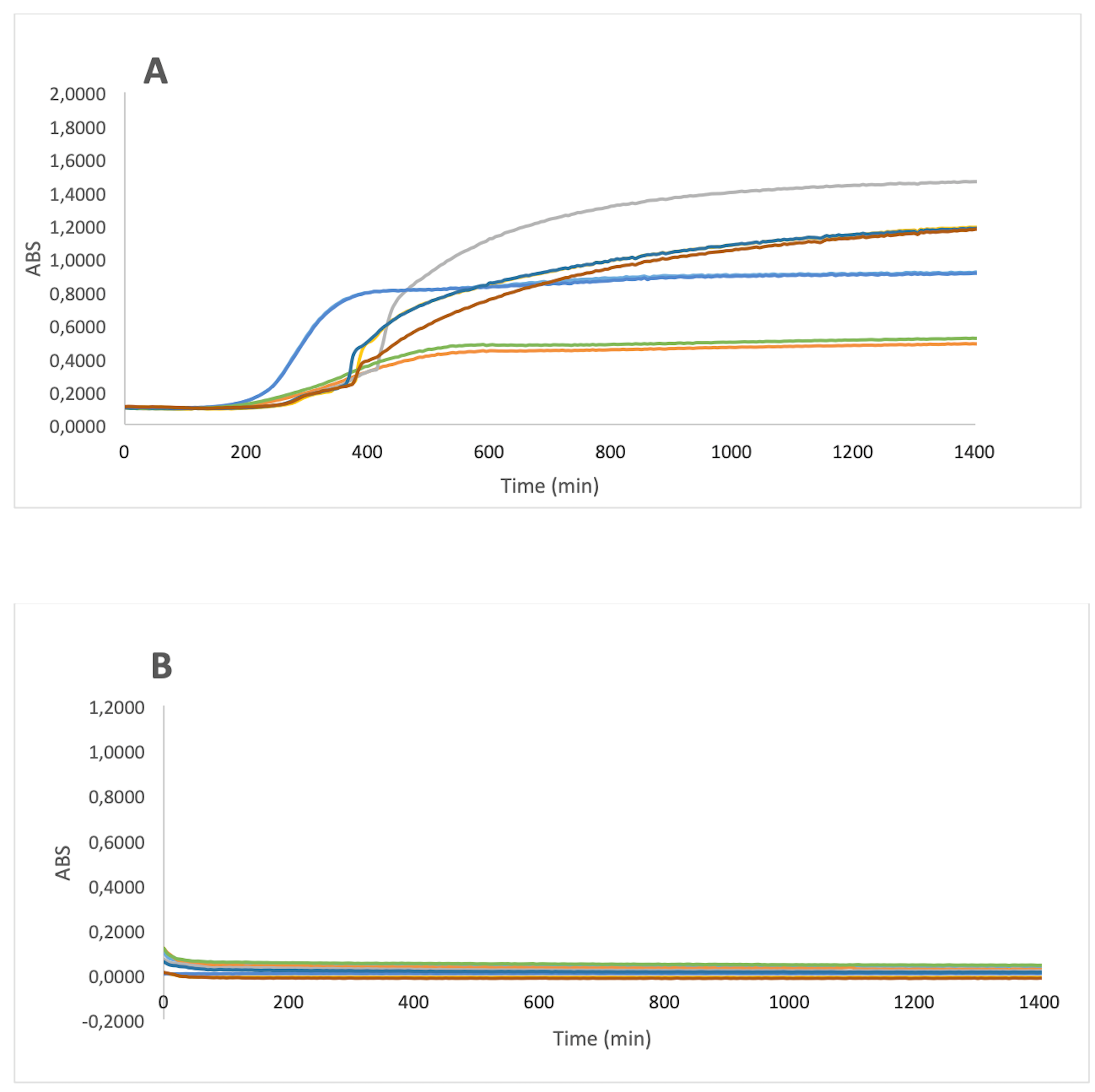
Nella Figura 1A sono presentate le curve di crescita di Staphylococcus aureus ATCC 29213, S. aureus 393, Pseudomonas aeruginosa L2, P. aeruginosa L4 e dei controlli.
È interessante notare che l’applicazione di IRON ANIMALS è stata in grado di sopprimere completamente la crescita batterica di tutti i microrganismi posti sotto osservazione (Figura 1B). L’efficacia battericida del preparato è stata definitivamente confermata dalla conta in piastra della crescita batterica, che ha evidenziato la completa scomparsa dei microrganismi in seguito all’introduzione del formulato. Si fa notare che l’eliminazione di S. aureus rappresenta un risultato di primaria importanza data la resistenza sviluppata da questo microrganismo ad uno dei disinfettanti più diffusi nella pratica clinica, la clorexidina.
Figura 1 – Crescita batterica in assenza (A) e in presenza (B) di IRON ANIMALS di Staphylococcus aureus ATCC 29213 (in colore blu), S. aureus 393 (in colore arancione), Pseudomonas aeruginosa L2 (in colore grigio), P. aeruginosa L4 (in colore giallo). ABS: Assorbanza misurata allo spettrofotometro espressa in unità arbitrarie ed equivalente alla densità ottica a 600 nm sottratta del bianco.
Casi studio per la valutazione dell’azione di IRON ANIMALS in vivo
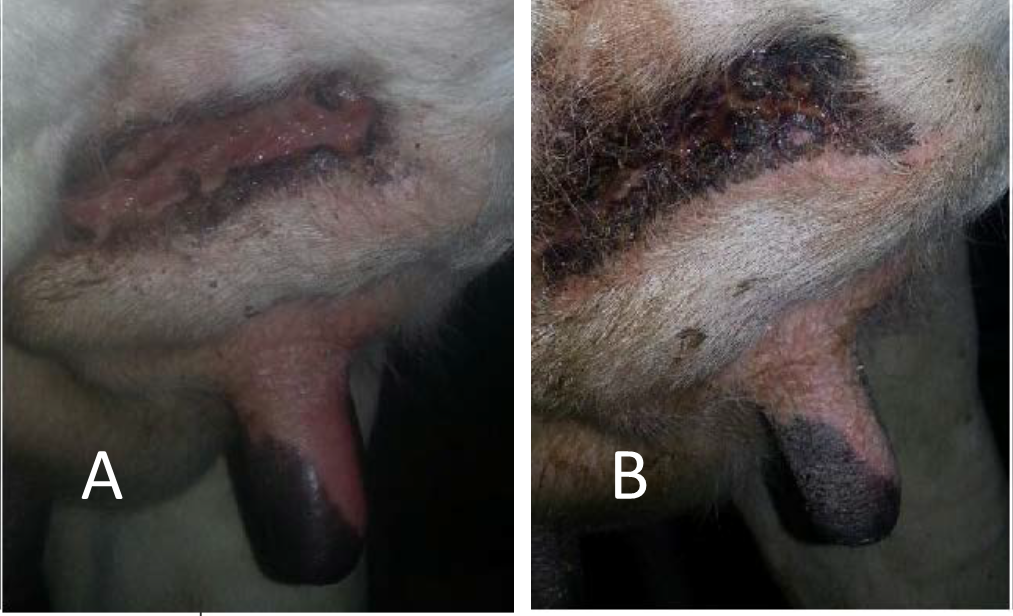
L’efficacia di IRON ANIMALS nell’eliminare i microrganismi può essere meglio apprezzata osservando il suo effetto su una piaga mammaria da decubito (vedi Figura 2).
Nel riquadro a sinistra è possibile osservare la presenza nella piaga di sangue rappreso e circostante flogosi, nonché la formazione di pus. La causa all’origine della formazione di pus è attribuibile ad infezione provocata da specifici microrganismi piogeni. Tra i batteri piogeni si possono trovare: Streptococchus, Meningococchus, Gonococchus e Staphylococchus. Dopo il trattamento della piaga con IRON ANIMALS, consistente in una somministrazione di pochi secondi del prodotto in forma spray (1-2 mL, ripetuta a distanza di due giorni), si evidenzia la scomparsa del materiale purulento a testimonianza dell’eliminazione della flora microbica, la riduzione della profondità della piaga, la formazione del tessuto cutaneo neo-cicatriziale, la reidratazione della pelle, nonché l’assenza di flogosi circostante (vedi Figura 2B).
Figura 2 – Piaga mammaria prima (A) e dopo (B) il trattamento con IRON ANIMALS.
Il medesimo risultato è stato osservato anche su una dermatite interdigitale (Figura 3 A) con presenza di infezione e pus. Ancora, dopo il trattamento con ossido di ferro colloidale nebulizzato per pochi secondi sulla ferita (1-2 mL) e ripetendo l’operazione a distanza di due giorni, il pus risulta assente e la lesione è cicatrizzata (Figura 3 B).
E’ importante sottolineare che, a differenza delle situazioni croniche trascurate degli esempi presentati che possono richiedere due o al massimo tre trattamenti per ottenere una completa guarigione nell’arco di una settimana, per analoghe patologie in fase iniziale è sufficiente un’unica somministrazione spray (1-2 mL) di IRON ANIMALS.
Figura 3 – Dermatite interstizionale, prima (A) e dopo (B) il trattamento con IRON ANIMALS.
Conclusioni
La resistenza sviluppata dai microrganismi ai comuni disinfettanti rappresenta un serio problema che si riflette su una sempre più urgente richiesta di alternative competitive rispetto alle soluzioni sinora adottate. Nel presente articolo è stata illustrata l’efficacia e l’azione antimicrobica aspecifica di IRON ANIMALS, che si è dimostrato in grado di eliminare batteri sia Gram-positivi (Staphylococcus aureus) che Gram-negativi (Pseudomonas aeruginosa). Nei casi studio presentati è stato mostrato come tale azione battericida dia luogo alla risoluzione di infezioni purulente ed alla guarigione di piaghe mammarie e dermatiti interstiziali. In quest’ottica IRON ANIMALS, grazie alla sua azione localizzata ed aspecifica, può rappresentare una valida alternativa alle sostanze attualmente utilizzate per la disinfezione della pelle animale, quali gli antibiotici. In questo contesto, la soluzione innovativa proposta da IRON ANIMALS può avere un elevato impatto in campo veterinario.
Autori
Massimiliano Magro, Gianfranco Gabai, Fabio Vianello – Dipartimento di Biomedicina Comparata e Alimentazione, Campus Agripolis, Università di Padova, viale dell’Università 16, Legnaro 35020 (PD).
Riferimenti bibliografici
Basso, C.R.; Crulhas, B.P.; Magro, M.; Vianello, F.; Pedrosa, V.A. A new immunoassay of hybrid nanomater conjugated to aptamers for the detection of dengue virus. Talanta 2019, 197, 482–490.
Hajipour, M.J.; Fromm, K.M.; Ashkarran, A.A.; Jimenez de Aberasturi, D.; de Larramendi, I.R.; Rojo, T.; Serpooshan, V.; Parak, W.J.; Mahmoudi, M. Antibacterial properties of nanoparticles. Trends Biotechnol. 2012, 30, 499–511.
Isola M., Piccinotti C., Magro M., Fasolato L., Vianello F., Menandro M.L., Memarian P., Rossi M., Falomo M.E. 2021. Colloidal iron oxide formulation for equine hoof disinfection. Animals, 11, 766.
Magro, M.; Vianello, F.; Braga, M. Aqueous Formulation Comprising Sds, Tca and Colloidal Suspension of Iron (III) for Use in the Topical Treatment of Micro-Organisms and Parasites. Patent PCT/IB2016/054295, 19 July 2016.
Magro, M.; Martinello, T.; Bonaiuto, E.; Gomiero, C.; Baratella, D.; Zoppellaro, G.; Cozza, G.; Patruno, M.; Zboril, R.; Vianello, F. Covalently bound DNA on naked iron oxide nanoparticles: Intelligent colloidal nano-vector for cell transfection. Biochim. Biophys. Acta Gen. Subj. 2017, 1861, 2802–2810.
Magro, M.; Baratella, D.; Bonaiuto, E.; de Almeida Roger, J.; Chemello, G.; Pasquaroli, S.; Mancini, L.; Olivotto, I.; Zoppellaro, G.; Ugolotti, J.; et al. Stealth Iron Oxide Nanoparticles for Organotropic Drug Targeting. Biomacromolecules 2019, 20, 1375–1384.
Mai, T.; Hilt, J.Z. Magnetic nanoparticles: Reactive oxygen species generation and potential therapeutic applications. J. Nanopart. Res. 2017, 19, 253.
Pelgrift, R.Y.; Friedman, A.J. Nanotechnology as a therapeutic tool to combat microbial resistance. Adv. Drug Deliv. Rev. 2013, 65, 1803–1815.




































































Scrivi un commento
Devi accedere, per commentare.